微生物所等揭示去泛素化酶OTUD1抑制肠炎发生新机制
来源:中检健康
编辑:中检健康
时间:2021-12-20
炎症性肠病(IBD)是一类免疫反应失调所致的反复发作的慢性肠道炎症性疾病,包括溃疡性结肠炎(UC)、克罗恩病(CD),多发于结肠和回肠末端。近几十年来,IBD发病率呈明显上升趋势,且目前临床上尚未找到有效根治IBD的治疗方案。肠道免疫系统能通过多种细胞和分子机制维持肠道免疫稳态,其紊乱可能导致多种炎症和免疫性疾病乃至肿瘤的发生。深入探寻肠道免疫微环境稳态的调控机制将为IBD等肠道免疫性疾病的防治提供新的分子标识。作为一种重要的去泛素化酶,OTUD1可调控自身免疫性疾病、病毒和真菌感染以及肠癌发生,但其在肠道炎症性疾病中的作用及调控机制尚不清楚。
近期,中国科学院微生物研究所刘翠华团队与军事科学院军事医学研究院张令强团队合作,发现去泛素化酶OTUD1能与RIPK1结合并通过去除其627位赖氨酸的K63多聚泛素化修饰,阻碍RIPK1对下游信号分子NEMO的招募及NF-κB信号通路的激活,进而抑制肠道免疫细胞中促炎细胞因子(包括TNF-α、IL-6和IL-1β等)的产生及肠炎发生。研究发现,葡聚糖硫酸钠(DSS)处理可诱导小鼠结肠组织中OTUD1的表达升高。在Otud1敲除小鼠中构建DSS结肠炎模型发现,Otud1敲除促进了小鼠肠道组织中促炎细胞因子的产生和肠炎发生。同时,小鼠骨髓移植实验也证明髓系细胞表达的OTUD1对肠炎的抑制作用是必不可少的。进一步的机制探寻发现,LPS能诱导OTUD1启动子区域的低甲基化从而促进OTUD1的高表达,之后OTUD1与RIPK1相互作用并通过去除RIPK1的627位赖氨酸的K63多聚泛素链,从而抑制其对NEMO的招募以及NF-κB信号通路的激活。研究还发现,相比于健康人群,UC患者肠道粘膜中OTUD1的表达更低,并且与UC相关的OTUD1 G403V突变体丧失了抑制RIPK1介导的NF-κB信号激活和肠炎发生的能力。
近期,中国科学院微生物研究所刘翠华团队与军事科学院军事医学研究院张令强团队合作,发现去泛素化酶OTUD1能与RIPK1结合并通过去除其627位赖氨酸的K63多聚泛素化修饰,阻碍RIPK1对下游信号分子NEMO的招募及NF-κB信号通路的激活,进而抑制肠道免疫细胞中促炎细胞因子(包括TNF-α、IL-6和IL-1β等)的产生及肠炎发生。研究发现,葡聚糖硫酸钠(DSS)处理可诱导小鼠结肠组织中OTUD1的表达升高。在Otud1敲除小鼠中构建DSS结肠炎模型发现,Otud1敲除促进了小鼠肠道组织中促炎细胞因子的产生和肠炎发生。同时,小鼠骨髓移植实验也证明髓系细胞表达的OTUD1对肠炎的抑制作用是必不可少的。进一步的机制探寻发现,LPS能诱导OTUD1启动子区域的低甲基化从而促进OTUD1的高表达,之后OTUD1与RIPK1相互作用并通过去除RIPK1的627位赖氨酸的K63多聚泛素链,从而抑制其对NEMO的招募以及NF-κB信号通路的激活。研究还发现,相比于健康人群,UC患者肠道粘膜中OTUD1的表达更低,并且与UC相关的OTUD1 G403V突变体丧失了抑制RIPK1介导的NF-κB信号激活和肠炎发生的能力。
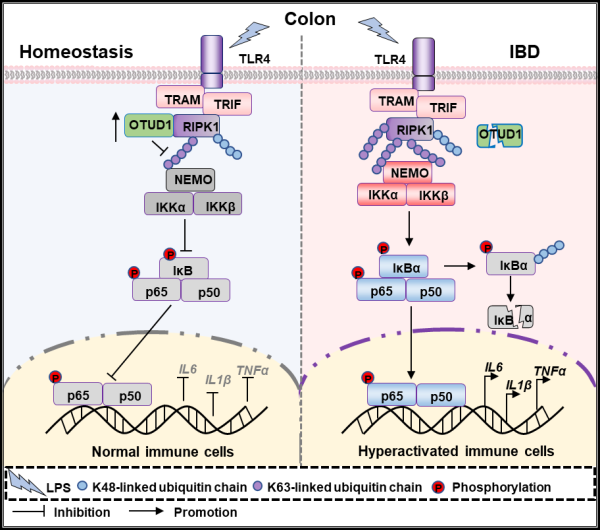
去泛素化酶OTUD1抑制肠炎发生的机制示意图。来源:论文链接
该研究揭示了去泛素化酶OTUD1通过去除RIPK1的K63多聚泛素链而抑制肠道免疫细胞中NF-κB通路介导的促炎细胞因子的产生进而抑制肠炎发生的分子机制,表明以OTUD1-RIPK1信号轴为靶点的免疫干预可能是治疗IBD的有效途径,该研究为肠道炎症性疾病的防治提供了潜在的干预新靶点。
相关成果发表在Cellular & Molecular Immunology上。研究得到国家生物安全特别项目、国家自然科学基金、中科院战略性先导科技专项和蛋白质组学国家重点实验室等资助。
论文链接:https://doi.org/10.1038/s41423-021-00810-9
文章来源:微生物研究所
(声明:本网站部分图片、文章来源于网络,本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将及时删除)
